
智享生物入选2024年江苏独角兽企业
2024年9月24日,江苏省生产力促进中心发布2024年江苏独角兽企业及瞪羚企业评估结果。智享生物荣获省级独角兽企业称号,为常熟市入选独角兽5家企业之一。 关于独角兽企业:省级独角兽企业是指在省级行政区划内,具有独立法人资格、无不良信用记录的企业。通常成立时间较短,获得过私募投资...

【瑞思普利】新三板挂牌获批
深圳瑞思普利生物制药股份有限公司于2024年6月28日收到全国股转公司下发的《关于同意深圳瑞思普利生物制药股份有限公司股票公开转让并在全国股转系统挂牌及定向发行的函》,同意公司股票公开转让并在全国股转系统挂牌及定向发行(证券简称:瑞思普利,证券代码:874344拟)。本次挂牌以新三板第四套标准进行申报,标志着瑞思...

激光电视年度最佳,【中科极光】荣获2024INDIEGOGO第五届年度峰会大奖
6月18日,在线上成交最火热的时候,富汇创投已投项目中科极光闪现深圳南山,凭借旗下产品CASIRSI H6,拿到了INDIEGOGO第五届年度峰会的——年度音频品类最佳项目大奖!作为全球最大的科创产品众筹平台INDIEGOGO,中国科创企业构筑全球出海品牌的第一站,本次主题为“创智者”,得到了深圳市南山区工业和信息化局、深圳市工业...

【凯思凯迪】I类新药CS060304中国IND获批
2024年6月18日,由凯思凯迪开发的具有独立自主知识产权的1类新药CS060304的临床试验申请(IND)获得国家药品监督管理局(NMPA)的默示许可, 此前已于2月在美国FDA获批临床。01关于CS060304CS060304是一种靶向甲状腺激素受体β(THR-β)的小分子激动剂,旨在用于治疗非酒精性脂肪性肝炎(NASH,又称MASH)患者。同靶点药物M...

【恒赛生物】中山研发中心开工建设
2024年5月21日,恒赛生物宣布中山研发中心正式开工。该中心位于中山市翠亨新区中山生命科学园,园区是粤港澳大湾区在生物医药产业方面的重要平台,集合医药研发、技术创新、服务平台和产业孵化等多重功能。在开工仪式上,恒赛生物的领导层对于支持公司发展的各方表示了深深的感激。建汇产业园董事长汪宝威、广州澳升总经理陈...

【瑞顺生物】全球创新 CD19-CAR-DNT细胞药治疗B细胞非霍奇金淋巴瘤注册Ⅰ期临床试验正式启动
2024年05月17日,广东瑞顺生物技术有限公司(以下简称 “瑞顺生物” )宣布,公司自主研发的全球创新CD19-CAR-DNT细胞药——RJMty19注射液治疗B细胞非霍奇金淋巴瘤的注册Ⅰ期临床试验已在三家研究中心正式启动。本注册临床研究项目由国内著名淋巴瘤治疗专家,上海交通大学医学院附属瑞金医院赵维莅教授牵头,南...
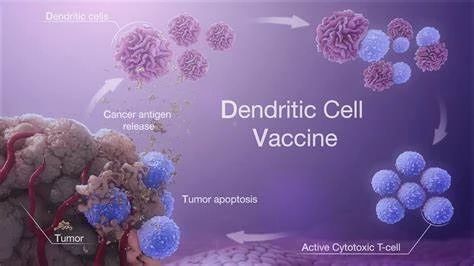
中国首款【恒赛生物】原创DC疫苗KSD-101获得FDA IND批件
2024年3月30日,恒赛生物宣布首发管线KSD-101获得美国食品药品监督管理局(FDA)授予新药临床试验(IND)许可,成为我国首款获得美国FDA IND批件的原创树突细胞疫苗(DC疫苗)产品。恒赛生物创始人兼CEO刘慧宁博士表示:“很高兴与大家分享这一喜讯, KSD-101的安全性和有效性在临床IIT研究中已得到初步验证,现在即将正式进入...
【瑞顺生物】现货通用型CAR-DNT细胞药第三个适应症治疗CD19阳性的成人复发/难治性B细胞急性淋巴细胞白血病获批临床。
2024年3月5日,广东瑞顺生物技术有限公司(下称 “瑞顺生物” )递交的RJMty19注射液(CD19-CAR-DNT细胞药)治疗CD19阳性的成人复发/难治性B细胞急性淋巴细胞白血病(受理号:CXSL2300853, 通知书编号:2024LP00519),获中国国家药品监督管理局(NMPA)药品审评中心(CDE)默认许可开展注册临床试验。本次IND申请获得CDE许...
瑞顺生物CD19-CAR-DNT细胞注射液治疗复发/难治性大B细胞淋巴瘤研究数据在柳叶刀子刊发表
2024年2月29日,柳叶刀子刊《eClinicalMedicine》正式发表了瑞顺生物CD19-CAR-DNT细胞(RJMty19注射液)治疗复发/难治性大B细胞淋巴瘤(LBCL)研究论文——CD19-CAR-DNT cells (RJMty19) in patients with relapsed or refractory large B-cell lymphoma: a phase 1, first-in-human study,此为CD19-CAR-DNT细胞注射液首次...

【凯思凯迪】I类新药CS060304获批进入临床研究
近日,凯思凯迪宣布由公司开发的具有独立自主知识产权的1类新药CS060304的临床试验申请(IND)获得美国食品药品监督管理局(FDA)默示许可。关于 CS060304CS060304是一种靶向甲状腺受体β(TRβ)的小分子激动剂,旨在用于治疗非酒精性脂肪性肝炎(NASH)患者。CS060304是一种强效选择性TRβ激动剂,特异性分布于肝组织。在...

【恒赛生物】完成数千万元A+轮融资
继2023年11月完成亿元级融资后,恒赛生物近日宣布再次获得数千万元A+轮融资,用于推进产品管线的拓展和临床申报以及中山研发中心和中试车间的建设。本次融资由翠亨集团、西湾投控、中山创投和成铭资本共同参与投资。恒赛生物成立于2018年,是致力于树突细胞疫苗(DC疫苗)研发与产业化的科技创新型企业、国家高新技术企业。...

瑞顺生物现货通用型CAR-DNT细胞药第二个适应症治疗复发/难治性B细胞非霍奇金淋巴瘤获批临床
“RJMty19注射液” 作为全球首款未经基因编辑获得通用型的现货CAR-DNT免疫细胞治疗产品的第二个适应症也正式进入注册临床试验。...

【凯思凯迪】入选“2023上海最具投资潜力50佳创业企业”榜单
12月7日,备受瞩目的“2023上海市最具投资潜力50佳创业企业”榜单在“外滩金融•上海国际股权投资论坛”上正式向社会揭晓,上海市地方金融监督管理局副局长葛平、上海市黄浦区人民政府党组成员、副区长林竞君出席论坛并致辞。凯思凯迪从百余家创业企业中脱颖而出,荣膺榜单。今年获评年度“最具投资潜力50佳”称号的创业企业...

【恒赛生物】完成亿元级A轮融资,富汇创投领投,劢柏资本担任独家财务顾问
恒赛生物顺利成功完成亿元级A轮融资,本次融资由富汇创投领投,勤智资本、凯骑康盈跟投,劢柏资本担任独家财务顾问。...

【百极优棠】小分子GLP-1促泌剂BPYT-01胶囊临床I期首剂量入组完成
百极优棠(广东)医药科技有限公司的小分子GLP-1促泌剂BPYT-01胶囊在上海市徐汇区中心医院成功完成首剂量入组。...

【瑞顺生物】现货通用型CD19-CAR-DNT细胞治疗复发/难治性B细胞非霍奇金淋巴瘤IND申请获CDE正式受理
瑞顺生物现货通用型CD19-CAR-DNT细胞治疗复发/难治性B细胞非霍奇金淋巴瘤IND申请获CDE正式受理...

【瑞顺生物】通用型CD19-CAR-DNT细胞治疗自身免疫性疾病IND申请获CDE正式受理
瑞顺生物宣布其全资子公司—瑞加美生物递交的“RJMty19注射液治疗复发/难治性自身免疫性疾病”IND申请得到国家药品监督管理局(NMPA)药品审评中心(CDE)正式受理(受理号:CXSL2300661)...

【领康时代】荣获“病原微生物实验室备案凭证(BSL-2)
领康时代获得由上海市奉贤区卫生健康委员会颁发的“上海市病原微生物实验室备案凭证(BSL-2)”证书,此举标志着领康时代在生物药品开发与生产以及实验室安全性方面得到进一步提升。...

【凯思凯迪】CS0159用于治疗原发性胆汁性胆管炎的中国临床II期研究完成首例患者给药
2023年8月30日,凯思凯迪(上海)医药科技有限公司宣布,CS0159治疗原发性胆汁性胆管炎(PBC)的中国临床II期研究已完成首例患者给药。...


